ПСА в деталях
 | Александр Викторович Говоров К.м.н., доцент кафедры урологии МГМСУ alexgovorov@newmail.ru |
 | Екатерина Олеговна Иванова Врач-невролог Научного центра неврологии РАМН kate-fileo@mail.ru |
История ПСА
Полвека назад одни ученые (M. Hara, G. Sensabaugh) искали маркеры, пригодные для ведения судебных дел по поводу сексуального насилия, другие (T.S. Li и C.G. Beling, S. Shulman и P. Bronson) – антигены, которые могли быть связаны с мужской инфертильностью. Были и исследователи, перед которыми стояла цель обнаружить маркеры злокачественных и доброкачественных изменений тканей предстательной железы.
Так или иначе, но все пришли к одному результату: к 80-му году прошлого столетия около 10 групп исследователей столкнулись с ПСА. Правда, у каждого ученого он именовался посвоему. Закрепившееся название досталось антигену от Ричарда Аблина (Richard J. Ablin), который в 1970 г. обнаружил ПСА, исследуя здоровые и поврежденные опухолью простаты.
Патент на открытие и идентификацию «очищенного человеческого антигена простаты» получил в 1984 г. Чу Мин (Chu Ming) – последователь доктора Аблина. Под руководством Чу Мина проведено не одно исследование, в которых он и его коллеги показали возможность использования ПСА для диагностических целей. Позже за свои работы он получил награды Американской ассоциации урологов (American Urological Association), Американского фонда урологических заболеваний (American Foundation for Urological Disease), Американского химического общества (American Chemical Society) и других профессиональных и научно-медицинских организаций.
В 1986 г. FDA (Food and Drug Administration) одобрило определение уровня ПСА у больных раком предстательной железы (РПЖ) иммуноферментным методом Hybritech Tandem PSA-Assay с целью наблюдения за эффектом лечения. А уже в 1994 г. – для скрининга и выявления РПЖ на начальной стадии.
С появлением ПСА в США наметилась четкая тенденция увеличения заболеваемости РПЖ. Причина – выявление РПЖ на ранних стадиях, в том числе и в ходе клинических исследований. Так, по данным NCI Surveillance Epidemiology and End Results (SEER) выявляемость РПЖ в 1989–1990 гг. составляла 16 %, а в 1990–1991 гг. – уже 30 %.
В России за период с 1998 по 2008 г. заболеваемость раком простаты тоже возросла более чем в 2 раза: с 15,28 до 33,69 на 100 тыс. населения. Такой скачок в российской онкостатистике также связан с улучшением качества диагностики.
Долгое время отсутствовали масштабные рандомизированные исследования, оценивающие преимущества и недостатки скрининга, из-за чего рекомендации многих медицинских обществ и организаций относительно скрининга РПЖ различались и до сих пор расходятся. Например, Американское общество по изучению рака (American Cancer Society) и Американская ассоциация урологов рекомендовали ежегодное определение общего ПСА крови и проведение пальцевого ректального исследования (ПРИ) у мужчин старше 50 лет, а также и у мужчин старше 40–45 лет в случае, если они принадлежат к группе повышенного риска (афроамериканцы, наличие РПЖ в семейном анамнезе и пр.).
Экспертами U.S. Preventive Services Task Force в октябре 2011 г. сделано заключение о нецелесообразности скрининга РПЖ при помощи определения уровня ПСА, что вызвало большую дискуссию в урологическом сообществе.
Например, Американская ассоциация урологов публиковала на своем сайте «мнение AUA» по данному вопросу, отметив, что «в будущем скрининг РПЖ должен быть сфокусирован на пациентах молодого возраста с высокой ожидаемой продолжительностью жизни», а также, что «обсуждение с пациентами вопросов лечения РПЖ должно включать тактику активного наблюдения с использованием современных молекулярных маркеров на различных этапах лечебно-диагностического процесса».
Полученные в 2009 г. по результатам исследования ERSPC (Европейское рандомизированное исследование скрининга РПЖ) новые данные о снижении смертности от рака простаты при использовании скрининга ПСА повлияли и, скорее всего, будут и дальше влиять на существующие стандарты и алгоритмы обследования пациентов, а также рекомендации профессиональных сообществ, посвященные данному вопросу. Так, в исследовании, проведенном в рамках ERSPC в г. Гетеборг, были показаны относительные различия в смертности от рака простаты в группе скрининга по ПСА и контрольной группе. Снижение смертности от РПЖ в скрининговой группе составило 27 % спустя 9 лет исследования и 56 % спустя 14 лет.
В 2011 г. появились новые сведения о том, что в протоколе ERSPC через 11 лет наблюдения скрининг привел к уменьшению частоты развития метастазов РПЖ на 41 %. Кроме того, продолжается целый ряд других проспективных рандомизированных мультицентровых исследований (например, PROTECT – Prostate Testing for Cancer and Treatment; PRIAS – Prostate Cancer Research International: Active Surveillance study; PIVOT – Prostate Cancer Intervention versus Observation Trial), которые позволят урологам больше узнать о скрининге и лечении РПЖ.
Что такое ПСА?
Это сериновая протеаза, принадлежащая семейству калликреинов. ПСА продуцируется клетками простаты и секретируется в семенную жидкость. Основная функция этого белка – разжижение семенной жидкости, которая в противном случае имела бы консистенцию густого геля. При нормальной архитектонике ткани простаты ПСА попадает в системную циркуляцию в очень малых количествах, в крови же этот белок присутствует в 2 формах – свободной (5–35 %) и связанной с ингибиторами протеаз (65–95 %).
Из-за нарушений нормальной структуры ткани железы ПСА попадает в кровь в больших количествах – его уровень в крови растет. Однако ПСА – это не онкологический, а простатспецифический маркер. Увеличение уровня ПСА в сыворотке крови может происходить как при наличии злокачественной опухоли простаты, так и в случае доброкачественной гиперплазии предстательной железы (ДГПЖ) или, например, инфекционного воспаления. Уровень ПСА в сыворотке крови также увеличивается после различных манипуляций, влияющих на простату, – массажа, биопсии, трансуретральной резекции предстательной железы, ПРИ и пр.
Увеличение концентрации ПСА в крови при РПЖ связано с нарушением архитектоники ткани железы и повышением проницаемости сосудов, но не с повышением выработки этого белка. Напротив, способность раковых клеток секретировать ПСА несколько ниже таковой у здоровых клеток.
От чего зависит уровень ПСА?
Риск наличия РПЖ варьирует в зависимости от уровня ПСА, в связи с чем возник вопрос, какую концентрацию ПСА считать пороговой. То есть такой, по достижении которой пациентам необходимо рекомендовать биопсию простаты. Учитывая тот факт, что 97 % здоровых мужчин в возрасте старше 40 лет имеют уровень ПСА 40 см3 соответственно (чувствительность 90 %): этот подход позволил бы компенсировать так называемый «эффект разведения», обусловленный большим объемом простаты.
Также известно, что у мужчин, получающих терапию ингибиторами 5-α-редуктазы, снижаются уровни общего и fПСА, в то время как % fПСА остается неизменным.
Предшественники ПСА
В 2010–2011 гг. появились новые данные о диагностической ценности [-2]проПСА и Индексе здоровья простаты PHI (Prostate Health Index).
Стоит объяснить, что проПСА, или [-7проПСА] – это нативная форма fПСА, в большей степени ассоциированная с заболеванием, чем ПСА и fПСА. Было обнаружено, что концентрация укороченных форм проПСА увеличена в периферической зоне раковой ткани по сравнению с тканью ДГПЖ. Помимо него в сыворотке присутствуют укороченные формы проПСА, в основном: [-5]проПСА, [-4] проПСА, [-2]проПСА.
На настоящий момент [-2]проПСА имеет наибольшую диагностическую ценность, так как его концентрация в экстрактах из опухолевой ткани самая высокая, а иммунохимическое окрашивание [-2]проПСА в раковых клетках интенсивнее, чем в доброкачественных. Более того, изоформа [-2]проПСА наиболее стабильна в условиях in vitro. Эти особенности уже находят применение в клинической практике. Так, недавно был разработан автоматизированный иммунохемилюминесцентный тест на определение [-2] проПСА в сыворотке крови – Access -2proPSA (Beckman Coulter). При этом наибольшая диагностическая ценность достигается путем консолидации показателей ПСА, fПСА и [-2] проПСА в один индекс – индекс здоровья простаты (Prostate Health Index – PHI).
Доказано, что применение индекса здоровья простаты с использованием результатов определения [-2]проПСА, ПСА и fПСА повышают чувствительность и специфичность при дифференциальной диагностике доброкачественных и злокачественных опухолей предстательной железы по сравнению с % fПСА. Так, по данным литературы, при 90 % чувствительности специфичность для % [-2]proPSA составила 33 %, при этом для % fПСА и ПСА – 17 % и 13 % соответственно.
Использование вышеуказанных показателей позволяет врачу принять обоснованное решение о направлении пациента на биопсию простаты или о ее нецелесообразности.
Трактовка и стандартизация ПСА
ПСА используется в определении рецидива РПЖ после радикальной простатэктомии. В связи с тем, что ПСА вырабатывается в основном клетками предстательной железы, в течение 21–30 дней после радикальной простатэктомии уровень маркера падает практически до нуля. Поэтому появление и нарастание уровня ПСА в крови через некоторое время после операции косвенно указывают на рецидив РПЖ.
В настоящее время считается, что повышение уровня ПСА ≥ 0,2 нг/мл свидетельствует о биохимическом рецидиве рака простаты. В соответствии с рекомендациями Европейской ассоциации урологов (EAU) уровень ПСА должен контролироваться через 3, 6 и 12 мес после радикальной простатэктомии; в случае же биохимического рецидива лечение должно быть начато прежде, чем уровень ПСА достигнет 0,5 нг/мл.
Как отмечено выше, возраст, раса и вес пациента могут влиять на уровень ПСА, с чем связаны некоторые трудности в трактовке результатов. Дополнительную сложность вносят и различия используемых тест-систем и калибраторов, порой – недостаточная специфичность используемых антител, а также нюансы, связанные с забором исследуемого материала и его хранением.
В 1994 г. метод определения ПСА, предложенный компанией Hybritech Corporation (ныне Beckman Coulter LLC), Hybritech Tandem PSA – «Total PSA» с калибровкой, основанной на внутреннем стандарте компании, был признан «золотым стандартом» определения ПСА для ранней диагностики РПЖ.
После многоцентрового проспективного клинического исследования, включавшего 6374 обследованных пациента, была установлена диа гностически значимая величина для определения рака простаты данным методом – 4 нг/мл. После этого многие производители диагностических тест-систем стали использовать метод Hybritech Tandem PSA как референсный, а в качестве диагностически значимого порогового значения величину 4 нг/мл, установленную для метода Hybritech. Но оказалось, что различия в антителах, используемых в технологии определения и форматах исследования альтернативных тестсистем, привели к получению большого количества ложноположительных результатов.
В 1995 г. A. Semjonov et al. показали, что различия в результатах исследования одних и тех же образцов сыворотки всеми доступными в Германии методами могут достигать 100 %. Возникла необходимость стандартизировать коммерческие тест-системы, и в 1999 г. Всемирная организация здравоохранения (ВОЗ) ввела стандарт калибровки 96/670.
При этом было установлено, что результаты, полученные при использовании калибровки по стандарту ВОЗ 96/670 на 20 % ниже по сравнению с результатами, полученными при использовании калибровки по стандарту Hybritech для наборов серии Access Hybritech Total PSA. Поэтому, согласно рекомендациям ВОЗ, пороговое значение для теста Access Hybritech Total PSA при калибровке по шкале стандарта ВОЗ 96/670 составило 3,1 нг/мл. Введение общего стандарта калибровки ВОЗ 96/670 позволило приблизиться к стандартизации методов определения ПСА, так как в итоге была достигнута прослеживаемость калибраторов разных тест-систем к единому стандартному первичному калибратору. Однако даже при проведении калибровки по шкале ВОЗ возможны дальнейшие расхождения, обусловленные различными антителами и другими биологическими материалами, используемыми при производстве тест-систем, а также перечисленными ранее особенностями. В связи с этим результаты, полученные в разных лабораториях на разных тест-системах, могут значительно отличаться, что особенно важно при мониторинге пациентов по уровню ПСА.
Источник
О чем говорит повышение ПСА у мужчин
Простатспецифический антиген — это опухолевый маркер, который применяется для диагностики рака и аденомы простаты. Его определяют в сыворотке крови. Повышение ПСА — один из недобрых «звоночков», говорящих о проблемах с предстательной железой. Причины плохого анализа могут быть разными.
Важно! Тест показывает нарушение деятельности железы, а не обязательное наличие рака или аденомы. В исследованиях рак простаты был обнаружен у 30% мужчин с повышенным ПСА. В остальных случаях наблюдались другие заболевания: простатит, инфекции мочеполовой системы и т. д.
Причины изменения уровня простатспецифического антигена
В зависимости от болезни могут изменяться причины, почему повышается ПСА у мужчин:
- рак простаты вызывает аномальную продукцию маркера опухолевыми клетками, а также повреждает базальные клетки;
- инфекция или воспалительный процесс могут вызывать повышение ПСА каждые три месяца или чаще, если их не лечить. Причина — повреждение эпителия и увеличение сосудистой проницаемости тканей;
- при аденоме простаты пса повышается из-за изменения объема органа и одновременной его компрессии разросшимися тканями;
- ишемия и инфаркт простаты, а также острые проблемы с мочеиспусканием, которые могут их вызывать, тоже приводят к плохим анализам. При них нарушается процесс кровообразования.
Как видите, причины, почему повышается ПСА, у каждого заболевания свои. Наличие перечисленных симптомов позволяет сделать более точный вывод о наличии или отсутствии рака у мужчины.
Интересно, что врачи против регулярного скрининга на ПСА здоровых мужчин. Считается, что это может привести к «гипердиагностике» и «избыточному лечению». Многие заболевания и процессы, вызывающие повышение ПСА, протекают бессимптомно годами, а медицинское вмешательство вполне может вызвать осложнения.
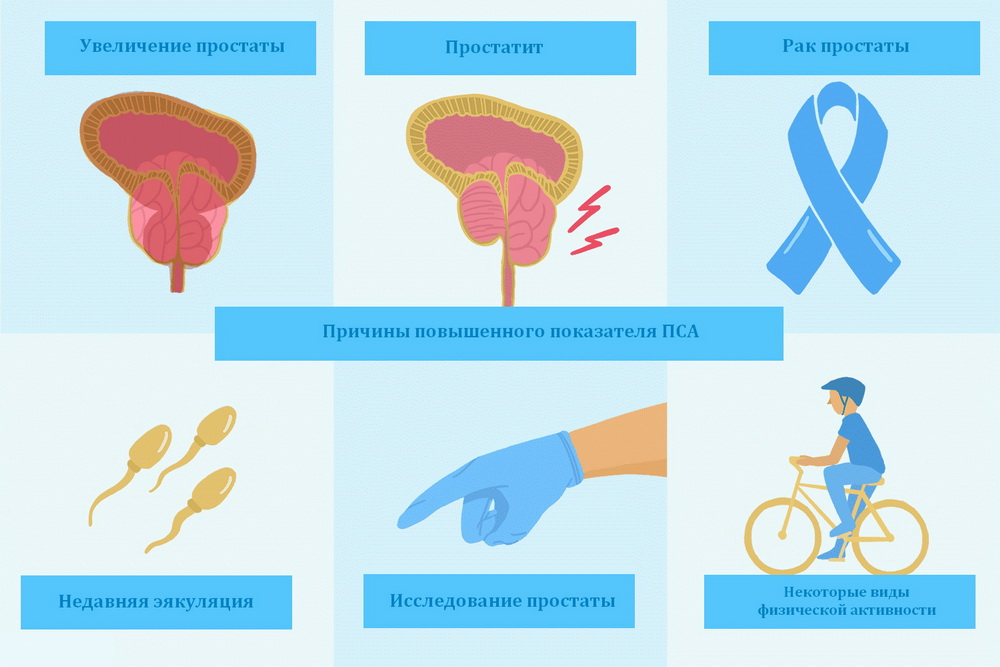
Что может резко повысить ПСА?
Нередко неуверенные в словах уролога мужчины сдают анализ несколько раз. Что делать, если на одном из тестов резко повысился ПСА? Волноваться не стоит, скорее всего, это связано с неправильной подготовкой к анализу. Суточные колебания маркера в сыворотке крови не значительны, но есть другие факторы, оказывающие влияние на результат. В каких случаях повышается ПСА у мужчин:
- недавняя эякуляция. Чтобы избежать ложного анализа, необходимо избегать ее примерно 48 часов до теста;
- массаж предстательной железы. Если он запланирован, то сдавать сыворотку крови нужно не ранее чем через три дня;
- трансректальное УЗИ. Между этой процедурой и тестом желательно выждать неделю;
- биопсия предстательной железы. Во время нее нарушается естественная работа органа. На восстановление нужно примерно 6 недель;
- трансуретральная резекция простаты. Она может сильно изменить показатель ПСА на полгода;
- после некоторых видов физической активности, например, активная велосипедная прогулка.
Правильная подготовка и учет всех сопутствующих факторов, будь то операции или исследования органа, позволяют врачу понять, что означает повышение ПСА в данном конкретном случае, корректно интерпретировать результаты.
Волнуетесь за свое здоровье? Есть неприятные симптомы? Клиника урологии имени Р. М. Фронштейна Первого Московского Государственного Медицинского Университета имени И.М. Сеченова (Государственный центр урологии) приглашает на прием к урологу. Врач тщательно вас обследует, направит на анализы, ответит на все вопросы. Звоните!
Акопян Гагик Нерсесович — врач уролог, онколог, д.м.н., врач высшей категории, профессор кафедры урологии ФГАОУ ВО Первый МГМУ им. И.М. Сеченова
Источник